Ваш регион, ?
МАВИТ в лечении больных хроническим простатитом и симптоматической аденомой предстательной железы
Введение
 Хронический простатит (ХП) и доброкачественная гиперплазия предстательной железы (ДГПЖ) являются частой
причиной дизурии, сопровождаются нарушениями опорожнения мочевого пузыря и удержания мочи – признаками,
которые обозначаются в литературе как «симптомы нижних мочевых путей» (СНМП) [23].
Хронический простатит (ХП) и доброкачественная гиперплазия предстательной железы (ДГПЖ) являются частой
причиной дизурии, сопровождаются нарушениями опорожнения мочевого пузыря и удержания мочи – признаками,
которые обозначаются в литературе как «симптомы нижних мочевых путей» (СНМП) [23].
У больных ДГПЖ сопутствующий воспалительный процесс в простате усугубляет симптомы нижних мочевых путей, снижает качество жизни пациентов и увеличивает вероятность развития острой задержки мочеиспускания [9,13,17].
По мнению клиницистов ХП обнаруживается у больных ДГПЖ с частотой от 72 до 84% случаев [6,14], а по исследованиям патоморфолог
ов до 96,7%. Продуктивные формы воспаления в предстательной железе чаще всего встречаются в виде интерстициального процесса, а воспалительный инфильтрат локализуется либо в строме органа, либо периацинарно [8].
Сочетание гиперплазии с острым воспалительным процессом в простате может достигать 30% [25].
Известно, что, помимо инфекционных агентов, в патогенезе ХП большое значение имеет местный фактор, связанный с нарушением микроциркуляции в железе и с ухудшением ее секреторно-динамических характеристик [7,16]. При хроническом воспалении в тканях железы наблюдаются дегенеративные изменения нервного аппарата и процесс запустения капилляров, что сопровождается расстройством тазовой гемодинамики и кровообращения в простате. Это явление получило название «ишемическая болезнь простаты» [24,26,25]. Толкование механизмов патогенеза ХП в данном аспекте во многом объясняет высокую эффективность и широкое применение методов физиотерапии в комплексном лечении хронического простатита, в том числе сопутствующего ДГПЖ [27, 30].
Наличие хронического воспаления в ткани простаты необходимо учитывать при определении лечебной тактики у больных ДГПЖ [9].
Недооценка воспалительного фактора может стать причиной гипердиагностики ДГПЖ и повлечь за собой выполнение аденомэктомии без достаточных на то показаний. С другой стороны, проведение трансуретральной резекции простаты (ТУР) или аденомэктомии по показаниям, но без адекватной предоперационной подготовки и лечения сопутствующего ХП, вызывает ряд воспалительных, геморрагических и тромбоэмболических осложнений в ближайшем послеоперационном периоде [12]. У таких больных после операции, как правило, длительно удерживаются симптомы нижних мочевых путей [11,28]. По этим причинам, лечение сопутствующего воспалительного процесса в простате у больных ДГПЖ имеет значение патогенетическое.
Терапия ХП проводится комплексно, с применением, в том числе, различных физических методов воздействия на простату [27]. Данные методы направлены на улучшение дренажной функции протоков предстательной железы и на улучшение микроциркуляции в зоне простаты.
Набор физиофакторов в последние годы расширился, а в практической работе появились новые медицинские устройства с возможностями проведения магнитотерапии, гипертермии, электрофореза, вибротерапии и др.[29]. Физиотерапевтические методы применяются и для лечения симптоматической ДГПЖ.
Термальные воздействия на простату (в частности, метод трансректальной гипертермии) используются в лечении больных ДГПЖ в периоде активного динамического наблюдения и входят в международные терапевтические стандарты [21]. Принятая терминология определяет гипертермию как поддерживаемый в тканях интервал температуры от +40°С до +45°С. Данный фактор эффективно воздействует на гиперплазированную ткань и вызывает активацию иммунитета и микроциркуляции в простате [1].
Такой же тепловой температурный режим с успехом применяется и в лечении ХП [1,2,14,15,27], что позволяет при ДГПЖ, осложненной воспалением простаты, использовать данный физический феномен как единый лечебный фактор.
Среди применяемых для лечения ХП физических факторов распространенным является магнитотерапия [4,29]. Применение постоянных или переменных низкочастотных магнитных полей имеет ряд преимуществ перед другими физиотерапевтическими методами. Магнитное поле обладает наибольшим числом действующих лечебных факторов, природно по своей сути и имеет минимальное количество противопоказаний. Оно рекомендуется к применению при хроническом простатите и не противопоказано при доброкачественных гормональнозависимых опухолях [20].
Воздействие на ткани и органы магнитным полем сопровождается широким спектром биологических эффектов: улучшаются параметры микроциркуляции, увеличивается просвет мелких сосудов, что способствует ускорению в них кровотока. За счёт раскрытия мелких лимфатических сосудов улучшается отток лимфы от органа и уменьшается отёк тканей.
Таким образом, локальное воздействие МП улучшает микроциркуляцию в органах и тканях с очевидным терапевтическим эффектом [16,22,27].
Периферическая нервная система реагирует на действие МП понижением чувствительности рецепторов, что обусловливает обезболивающий эффект. Противовоспалительное и анальгетическое действие МП сохраняется после курсовых воздействий до 30-45 дней [5].
Устранению конгестивных явлений в простате, снижению СНМП активно способствует стимуляция сократительной способности мышечных элементов предстательной железы и тазового дна. Восстанавливается при этом мышечный тонус и улучшается эвакуация простатического секрета [4,29].
Такая стимуляция может проводиться с помощью локального действия механической вибрации, создаваемой в перипростатических тканях и в предстательной железе.
Помимо названных, для лечения ХП и ДГПЖ широко применяются и другие факторы физического воздействия: электростимуляция предстательной железы, инфракрасное лазерное излучение, микроволновая СВЧ – терапия и др. [4,10,21].
Материалы и методы
С целью повышения эффективности, качества и комфортности комплексного лечения ХП нами применялось физиотерапевтическое устройство для лечения воспалительных заболеваний предстательной железы – АЛП-01 «ПРА» («МАВИТ»). Этот медицинский прибор (патент РФ № 52556) способен локально воздействовать на простату одновременно тремя физическими лечебными факторами. В их числе гипертермия, импульсное магнитное поле (МП) и механическая вибрация.
Устройство состоит из источника питания, подключаемого к бытовой электрической сети, и рабочего элемента – ректального зонда-аппликатора, соединенного с блоком питания. Рабочий элемент имеет конфигурацию суппозитория с рабочей поверхностью, адаптированной по форме к особенностям синтопии прямой кишки и простаты.
Физические влияния, создаваемые локально в области простаты рабочим элементом устройства «МАВИТ», имеют определенные параметры с биотканевыми эффектами терапевтического спектра действия. В режиме лечения на рабочей поверхности аппликатора, контактирующего с перипростатическими тканями и находящегося в непосредственной близости от простаты, создается и поддерживается постоянная температура от +42,0°С до +42,5°С. Гипертермия улучшает внутритканевую микроциркуляцию (в том числе в области перипростатических тканей и нервных сплетений), повышает интенсивность обмена веществ в тканях, ускоряет процессы элиминации тканевых метаболитов и оказывает спазмолитическое действие [2,7,22,27].
Кроме того, рабочий элемент является излучателем импульсного низкочастотного МП с магнитной индукцией, меняющейся в диапазоне от 0,5мТл до 15мТл. Режим частоты МП приближен в устройстве «МАВИТ» к параметрам магнитного поля биообъектов, что ориентировано на уровень резонансных реакций биологических тканей [18,22]. Рабочий элемент медицинского устройства является также источником механической вибрации, генерируемой с переменной частотой от 25 до 100 Гц.При проведении процедуры ректальный зонд-аппликатор помещается в чехол из латекса и вводится в прямую кишку пациенту, располагающемуся на кушетке в положении «лежа на спине» или «лежа на боку».
Продолжительность лечебного сеанса составляет 30 минут; курс лечения состоит из 7-9 процедур, выполняемых через день.
Клиническая эффективность устройства «МАВИТ» изучена нами в комплексном лечении 45 пациентов с хроническим простатитом. Всем больным проводилось общеклиническое и специальное обследование, включающее суммарную оценку симптомов при заболеваниях простаты по международной шкале IPSS, оценку качества жизни (QOL). Изучались показатели урофлоуметрии с оценкой объема остаточной мочи, проводилось пальцевое ректальное исследование простаты с микроскопическим и бактериологическим исследованием секрета простаты, ультразвуковое исследование (УЗИ) мочевого пузыря, простаты, в том числе с помощью трансректального датчика. Всем пациентам в возрасте 40 и более лет проводилось исследование уровня простатспецифического антигена в плазме крови с целью исключения рака простаты. Контроль эффективности терапии ХП осуществлялся непосредственно после проведенного курса лечения с применением устройства «МАВИТ» и в последующие 12 месяцев после лечения. По результатам предварительного обследования больные были разделены на две группы.
Первая (основная) группа (ДГПЖ+ХП) состояла из 25 пациентов, у которых была диагностирована доброкачественная гиперплазия простаты I-II ст., осложнённая хроническим простатитом. Средний возраст больных в этой группе был равен 64,28±9,9 (от 45 до 87) лет. При постановке диагноза у 6 больных в соответствии с классификацией NIH USA (1995) определена II клиническая категория сопутствующего ХП, у 7 пациентов - категория IIIA и у 12 – IIIB.
Во вторую группу (ХП) вошли 20 больных хроническим простатитом в возрасте от 39 до 51 лет (M=41,2±6,21), среди которых у 10 пациентов клиническая категория ХП определена как II, а у десяти других - как IIIA.
Обе клинические группы (ХП и ДГПЖ+ХП) объединяют не только процесс воспаления, но и характерные дизурические явления - симптомы нижних мочевых путей. При ХП в воспалительный процесс закономерно вовлекается зона мочепузырного треугольника, которая участвует в формировании позыва к мочеиспусканию [9]. В результате, у больных обнаруживаются симптомы гиперрефлексии детрузора, что наблюдается и в начальных стадиях ДГПЖ.
Все пациенты получали комплексную терапию, включающую прием простатотропных антибактериальных препаратов, противовоспалительных средств, неспецифических иммунокорректоров и адаптогенов.
Для оценки биотканевого влияния устройства «МАВИТ» на кровообращение ПЖ и окружающие ткани у 10 больных из второй группы (ХП) до и после физиотерапевтического сеанса проводилось трансректальное ультразвуковое исследование ПЖ в режиме цветного доплеровского картирования. Изучалась линейная пиковая скорость кровотока, индекс периферического сосудистого сопротивления, а также плотность органного сосудистого рисунка.
Результаты
Результаты лечения больных прослежены в обеих группах в сроки от 3 до 12 месяцев. В ближайшие 1,5-2 месяца у всех больных отмечено уменьшение или исчезновение СНМП, улучшился акт мочеиспускания. Практически у всех больных уменьшились или исчезли боли в области гениталий.
В первой группе больных (ДГПЖ+ХП) изучены основные параметры мочеиспускания, определяющие СНМП, а также индекс качества жизни. Все показатели фиксировались в анкетах больных до начала лечения, оценивались в динамике после проведенной терапии и были сопоставлены с данными о состоянии больных на этапе 6 месяцев после окончания курса лечения с применением устройства «МАВИТ». Результаты представлены в таблице 1.
Таблица 1. Динамика некоторых клинических показателей у больных ДГПЖ с сопутствующим ХП, получавших лечение с применением устройства локальной физиотерапии «МАВИТ» (n=25)
| Показатель (среднее значение) | До лечения | После лечение (6 мес.) |
| Количество ночных мочеиспусканий | 3,88±1,49 | 2,74±0,34 |
| Объём остаточной мочи (мл.) | 58,5±37,4 | 21,5±11,85 |
| Максимальная объёмная скорость потока мочи (Qmax), мл/сек. | 10,09±3,01 | 13,923±3,16 |
| Балл I-PSS (S) | 18,48±5,1 | 11,2±2,54 |
| Индекс оценки качества жизни (QOL) | 4,04±0,84 | 2,68±0,47 |
Все пациенты отметили уменьшение количества ночных мочеиспусканий при снижении среднего значения эпизодов ноктурии, практически, в 1,5 раза.
Различия сравниваемых величин статистически высоко достоверны (р<0,001).
Объём остаточной мочи уменьшился по средним значениям на 37,0 см 3 (при p>0,01). Максимальная скорость потока мочи (Q max) к шестому месяцу наблюдения за пациентами составила 13,923±3,16 мл/с. Различия со средней исходной величиной статистически достоверны при доверительном коэффициенте t=2,8 (0,01<p<0,05).
Сумма симптомов нижних мочевых путей по шкале I-PSS у больных первой группы через шесть месяцев наблюдения снизилась на 7,28 баллов (р=0,05 при t=2,43), что демонстрирует положительную динамику течения заболевания (табл. №1). Наряду с уменьшением обструктивных симптомов наблюдалась также динамика снижения ирритативных проявлений болезни.
Пациенты отмечали исчезновение императивных позывов к мочеиспусканию, уменьшение количества мочеиспусканий при относительной стабильности значений суточного диуреза.
В первой группе, при общей положительной клинической динамике, у одного больного через 8 месяцев после лечения развилась острая задержка мочеиспускания, спровоцированная приёмом алкоголя, что потребовало хирургического вмешательства. Больному по неотложным показаниям выполнена одноэтапная аденомэктомия. Гистологическое изучение удалённой ткани подтвердило признаки хронического воспаления в простате, которые выражались в диффузной лимфоцитарной и гистиоцитарной инфильтрации, преимущественно периваскулярного характера с различной степенью трансформации в клетки фибробластического ряда и очаговым фиброзом. Выявлены лимфоидные скопления типа фолликулов, сосредоточенные преимущественно вблизи разрушенных кистозных полостей, с диффузией секрета в строму железы.
При оценке результатов лечения больных ДГПЖ+ХП нами отмечено, что после окончания комплексной терапии объём предстательной железы у всех пациентов имел тенденцию к уменьшению, в среднем, по данным УЗИ, на 2,37±1,1 см 3 (p<0,05). Последнее, вероятно, можно объяснить стиханием воспалительного процесса и уменьшением конгестивных явлений в предстательной железе под влиянием лечения.
Во второй группе (ХП) в течение первого месяца после лечения у 17 больных (85%) наблюдалось снижение болевого синдрома. Спустя 6 месяцев после лечения болевые ощущения сохранились у 2-х пациентов (10%). Симптомы нижних мочевых путей характеризуются следующей динамикой. До лечения среднее количество мочеиспусканий у одного больного в сутки составляло 7,8±1,1 с дискомфортом и резью в уретре в конце акта мочеиспускания. Через 6 мес. при контрольном обследовании выявлено уменьшение симптомов ирритативного характера и количества мочеиспусканий в сутки до 5,4±1,4. Различия сравниваемых средних величин существенны, но статистически недостоверны при вероятности ошибки более 40% (р>0,05; t=1,78).
Максимальная объёмная скорость потока мочи (Q max.) у больных данной группы возросла к 6-ому месяцу после лечения, в среднем, до 22,1±1,1мл/с при исходной средней величине М=17,9±1,6мл/с. Различия средних статистически достоверны (0,01<p<0,05). Дискомфорт при мочеиспускании в оцениваемый период времени сохранялся лишь у 2-х больных. В клинической структуре болезни у этих двух пациентов прослеживались признаки психосоматизации заболевания.
При контрольном пальцевом ректальном исследовании болезненности и очаговой инфильтрации в перипростатических тканях и в простате не было выявлено ни в одном наблюдении, что совпадало с положительной динамикой результатов УЗИ. На фоне улучшения самочувствия у больных в обеих группах зафиксировано значительное улучшение или нормализация ряда клинических показателей.
Для оценки состояния кровотока в предстательной железе после сеанса локальной физиотерапии на устройстве «МАВИТ» у 10 больных второй группы (ХП) проведено трансректальное ультразвуковое исследование ПЖ в режиме цветного доплеровского картирования до и после лечебного сеанса, показавшее улучшение микроциркуляции в ткани предстательной железы.
Применение аппарата «МАВИТ» приводит к выраженной реакции в виде усиления кровообращения по всему сосудистому коллектору (см. рис. 1 и 2).
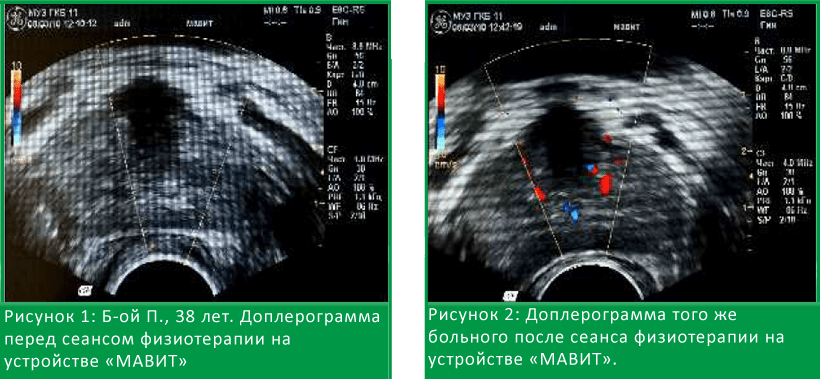
Средний показатель линейных пиковых скоростей в изученной подгруппе увеличился в 1,1 раза, уменьшилась величина индекса резистентности в 1,2 раза в сравнении с исходными данными. Средний показатель плотности сосудистого рисунка увеличился более чем в 2,5 раза.
Лечение с применение устройства «МАВИТ» было предложено оценить самим пациентам по 5-балльной шкале. Негативных оценок от применения «МАВИТ`а» в изученной группе больных получено не было. Практически все пациенты отметили высокую эффективность процедур и удобство использования метода, в том числе и в амбулаторных условиях (табл. 2).
Таблица 2. Субъективная оценка, данная пациентами, об эффективности лечения с применением устройства «МАВИТ»
| Оценка | Отлично | Хорошо | Удовлетворительно | Не связывает эффект | Ухудшение |
| Распределение пациентов (в %) | 41,7 | 58,3 | 0 | 0 | 0 |
Терапевтический эффект локального физического воздействия, оказываемого устройством «МАВИТ», в комплексном лечении ХП мы связываем с улучшением микроциркуляции в предстательной железе и в перипростатических тканях, с обезболивающим эффектом вибрационного фактора и импульсного МП, с уменьшением спастического и отёчного компонентов, сопровождающих воспалительный процесс в простате. Эти эффекты реализуются в комплексном одновременном действии факторов гипертермии, вибрации и импульсного магнитного поля на ткань предстательной железы и нервные структуры, входящие в состав тазового нервного сплетения и в простатическое сплетение (plexus prostaticus).
Последнее располагается в перипростатической ткани по задней и боковым поверхностям простаты и хорошо доступно для рабочей части зонда-аппликатора устройства «МАВИТ» в рабочем режиме [7,16]. Ряд ветвей простатического сплетения иннервирует предстательную и мембранозную части мочеиспускательного канала, некоторые из них входят в состав нервов пещеристых тел полового члена (nn. cavernosi penis). Нервные стволы, проходящие через простатическое сплетение, участвуют в двигательной иннервации mm. levator ani и поперечнополосатого сфинктера уретры – образований, которые осуществляют пассивный и активный контроль акта мочеиспускания. Все названные структуры при патологических процессах в предстательной железе, в том числе при ДГПЖ и хроническом простатите, в большей или меньшей мере участвуют в формировании симптомов нижних мочевых путей. Локальное физиотерапевтическое воздействие на предстательную железу, её иннервационный аппарат и перипростатическую ткань усиливает эффекты антибактериального и противовоспалительного лечения ХП, что в совокупности купирует симптомы дизурии – основные для пациентов с симптоматической ДГПЖ.
В патогенезе симптоматической ДГПЖ сопутствующий ХП нередко является причиной симптомокомплекса СНМП. Проведение комплексной противовоспалительной терапии ХП снижает проявление СНМП. У больных симптоматической ДГП с сопутствующим ХП такой подход в консервативной стадии заболевания имеет патогенетическое значение и, при необходимости, позволяет адекватно подготовить больного с ДГПЖ к хирургическому лечению.
Полученные данные позволяют рекомендовать устройство МАВИТ для лечения хронического простатита у больных доброкачественной гиперплазией простаты I-II ст. Лечение с применением устройства МАВИТ должно проводиться вне стадии активного воспаления в простате в комплексе с антибактериальными, противовоспалительными препаратами, адаптогенами, иммунокорректорами и симптоматическими средствами.
Лечение больных может проводиться в стационаре, в амбулаторных условиях, а также в домашних условиях под наблюдением уролога.
Литература:
- Аполихин О.И., Сивков А.В., Ощепков В.Н. Термальные неэндоскопические методы лечения ДГПЖ./Сб. «Доброкачественная гиперплазия предстательной железы». //Под ред. акад. РАМН Н.А. Лопаткина, М., 1999, С.134-149.
- Арнольди Э.К. Простатит: опыт, проблемы, перспективы.- Харьков.- «Каравелла».- «Питер-Т».- «Неофит»,1997.- 223с.
- Берклайд П.М., Лямин Б.А., Неменова А.А., // Урол. и нефрол.- 1989.- №3.- С.73-78.
- Голубчиков В.А., Кондаков А. Лечение простатита: новые подходы.- МГ, 1998, №55.- С.10-11.
- Демецкий А.М. Медико-биологическое обоснование применения магнитных полей в практике здравоохранения.- Ленинград, 1989.-157с.
- Жиборев Б.Н., Ракчеев Б.Ю., Салынов А.В., Барсук А.Н. Трансуретральная микроволновая терапия как метод выбора в лечении доброкачественной гиперплазии простаты./ Сб. научн. тр. РязГМУ «От коллатерального кровообращения к органосберегающим операциям»./Под ред. проф. В.Г. Аристархова и проф. Ю.Б. Кириллова, Рязань, 1999.- С.125-127.
- Жиборев Б.Н., Салынов А.В., Ракчеев Б.Ю., Григорьев В.М., Глуховец И.Б. Лечение хронического неспецифического уретрита и простатита новыми аппаратами локального теплового воздействия./Ж. «Урология», 2000, №3, С.37-41.
- Кудрявцев Ю.В., Романова Л.М. Морфологические изменения в ткани предстательной железы при доброкачественной гиперплазии./Сб. «Доброкачественная гиперплазия предстательной железы» // Под ред. акад. РАМН Н.А. Лопаткина, М., 1999.- С.37-45.
- Кучук Я.И., Лямин Б.А. Особенности клинической картины и лечебной тактики при аденоме простаты и сопутствующем хроническом простатите./ Сб. научн. тр. «Воспалительные заболевания почек, мочевых путей и мужских половых органов».//Под ред. проф. А.Л. Шабада и проф. В.Г. Горюнова, М., 1991.- С.131-137.
- Ловцов В.В., Митряев Ю.И., Блюмберг Б.И., Волин М.В. и др. Метод комбинированной консервативной терапии в лечении больных доброкачественной гиперплазией простаты./ Сб. научн. тр. РязГМУ «От коллатерального кровообращения к органосберегающим операциям» / Под ред. проф. В.Г. Аристархова и проф. Ю.Б. Кириллова, Рязань, 1999.- С. 116-118.
- Лоран О.Б. Диагностика и дифференциальная диагностика доброкачественной гиперплазии предстательной железы. / Сб. «Доброкачественная гиперплазия предстательной железы». //Под ред. акад. РАМН Н.А. Лопаткина, М., 1999.- С.56-70.
- Минаков Н.К., Мкртчян Г.Г. Результаты амбулаторной предоперационной терапии воспалительных заболеваний мочеполовых органов у больных аденомой простаты./ Сб. научн. тр. «Воспалительные заболевания почек, мочевых путей и мужских половых органов». //Под ред. проф. А.Л. Шабада и проф. В.Г. Горюнова, М., 1991.- С.169-175.
- Новиков И.Ф., Александров В.П., Артёмов В.В. «Эндоскопическая электрохирургия в урологии»- Санкт-Петербург, 2001, 187с.
- Редькович В.Н., Чиненный В.Л. Профилактика острого эпидидимоорхита в урологической клинике./Сб. научн. тр. «Воспалительные заболевания почек, мочевых путей и мужских половых органов». //Под ред. проф. А.Л. Шабада и проф. В.Г. Горюнова, М., 1991.- С.175-182.
- Репродуктивное здоровье. В 2 т., Т 1. «Общие инфекции». Пер. с англ. / Под ред. Л.Г. Кейта, Г.С. Бергера, Д.А. Эдельмана.- М.: «Медицина», 1988, 443с.
- Руководство по андрологии. / Под ред. О.Л. Тиктинского.-Л.: «Медицина».- С.1990.
- Сегал А.С., Долгопятов Д.Г., Ахтаев Г.Г. Лечение простатодинии альфа-1-адреноблокаторами //Андрология и генитальная хирургия, 2000, №2.- С.100-101.
- Системы комплексной электромагнитотерапии./ Уч. пособие для ВУЗов под ред. Беркутова А.М., Жулева В.И., Кураева Г.А., Прошина Е.М.-М.: ”БИНОМ”, 2000г.- 376 с.
- Справочник по физиотерапии. /Под ред. Ясногородского.- М.: «Медицина», 1992.
- Сучкова Ж.Н. Локальная магнитотерапия./МГ, 2001, №62.-С.9-13.
- Трапезникова М.Ф., Базаев В.В. Классификация методов лечения доброкачественной гиперплазии простаты. /Сб. «Доброкачественная гиперплазия предстательной железы». //Под ред. акад. РАМН Н.А. Лопаткина, М., 1999.- С.84-90.
- Улащик В.С. «Новые методы и методики физической теории»- «Беларусь».- Минск, 1986 .
- Verhamme K.M.C., Dieleman J.P., Bleumink G.S., J. van der Lei, Sturkenboom M.C.J.M. Incidence and Prevalence of Lower Urinary Tract Symptoms Suggestive of Benign Prostatic Hyperplasia in Primary Care – The Triumph Project // European Urology, 42 (2002).- P.323-328.
- Pinggera G.M., Schuster A., Pallwein L., Frauscher F. et al. Chronic ischemia of the Lower Urinary Tract – a possible cause of Lower Urinary Tract Symptoms//XIX Congress of the EAU. Abstract Book. – European Urology Supplements, Vol.3 (2004), No.2. - P.21.
- Коган М.И., Чибичян М.Б., Ильяш А.В., Лаптева Т.О. Активность тканевого воспаления в предстательной железе при доброкачественной гиперплазии и раке простаты. //Материалы VI Российского конгресса «Мужское здоровье».- М.: 2010.- С. 145-146.
- Абоян И.А., Абоян В.Э. Грачев С.В. и др. Проблемы с мочеиспусканием у пациентов с синдромом хронической тазовой боли.//Материалы VI Российского конгресса «Мужское здоровье».- М.: 2010.- С.15-16.27. Глыбочко П.В., Чураков А.А., Попков В.М., Блюмберг Б.И. Хронический инфекционный простатит.//Материалы VI Российского конгресса «Мужское здоровье».- М.: 2010.- С.24-35.
- Камалов А.А., Баблумян А.Ю., Белик С.М.Прогнозирование вероятности сохранения ирритативных расстройств мочеиспускания у больных доброкачественной гиперплазией предстательной железы после аденомэктомии. //Материалы VI Российского конгресса «Мужское здоровье».- М.: 2010.- С.137-138.
- Каприн А.Д., Миленин К.Н., Трихлеб В.И. Опыт комплексного применения аппаратов АЭЛТИС – синхро -02 и АМЛТИС – синхро -01 «Яровит» в лечении ХБП. //Материалы VI Российского конгресса «Мужское здоровье».- М.: 2010.- С.72-74.
- Назаров Т.Н., Ризоев Х.Х. Оценка кровотока предстательной железы у больных хроническим обструктивным простатитом. //Материалы VI Российского конгресса «Мужское здоровье».- М.: 2010.-С.86-87.
Источник: Научно-практический журнал "Урология" №6 6'2011